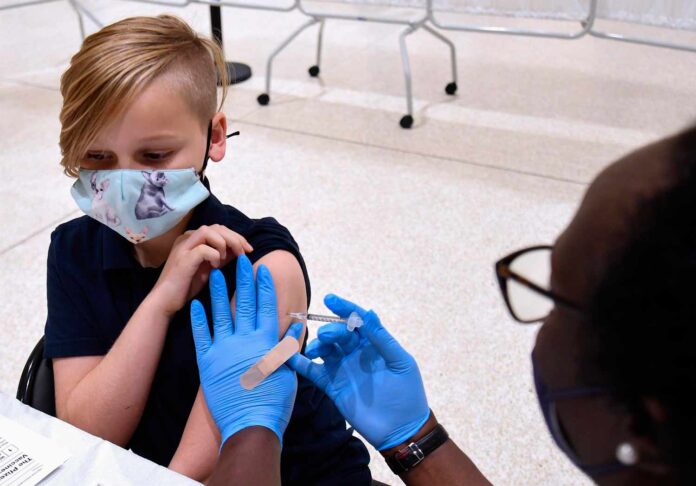
El CHMP concluye que los beneficios de la vacuna ‘Comirnaty’ de Pfizer en niños de 5 a 11 son mayores que los riesgos, “particularmente en aquellos con condiciones que aumentan el riesgo de graves COVID-19”
El Comité de Medicamentos de Uso Humano (CHMP, por sus siglas en inglés) de la Agencia Europea del Medicamento (EMA, por sus siglas en inglés) ha decidido, en una reunión extraordinaria celebrada este jueves, dar el visto bueno a la vacuna de Pfizer contra la COVID-19 en niños de 5 a 11 años.
Según acaba de informar en un comunicado, la dosis será inferior a la utilizada en personas de 12 años o más (10 ug frente a 30 ug), y al igual que en el grupo de mayor edad, se administra en dos inyecciones en los músculos de la parte superior del brazo, con tres semanas de diferencia.
Tras el análisis de los estudios facilitados por la compañía, el CHMP concluye que los beneficios de la vacuna ‘Comirnaty’ de Pfizer en niños de 5 a 11 son mayores que los riesgos, “particularmente en aquellos con condiciones que aumentan el riesgo de graves COVID-19”. Por tanto, el CHMP enviará ahora su recomendación a la Comisión Europea, que emitirá una decisión final.
Esta decisión se produce en medio de un gran aumento de casos de COVID-19 en toda Europa, principalmente por la escasa cobertura de vacunación en algunos países y porque el colectivo de menores de 11 años aún no ha podido recibir la vacuna.
En España, de hecho, los menores de 11 años son los que acumulan una mayor incidencia acumulada a 14 días por 100.000 habitantes, con 203,57, según los datos del Ministerio de Sanidad publicados ayer, muy por delante del siguiente grupo, las personas entre 40 y 49 años, que se sitúan en 155,91.
La vacuna de Pfizer, ‘Comirnaty’, está autorizada en niños de 5 a 11 años en Estados Unidos desde hace casi un mes. De acuerdo con los datos publicados por la Administración de Alimentos y Medicamentos de Estados Unidos (FDA, por sus siglas en inglés), la vacuna tuvo un 90,7 por ciento de efectividad en la prevención de la COVID-19 en este grupo etario.
EN QUÉ SE BASA LA APROBACIÓN
El comité ha basa su aprobación en un estudio en niños de 5 a 11 años mostró que la respuesta inmune a ‘Comirnaty’ administrada a una dosis más baja (10 ug) en este grupo de edad fue comparable a la observada con la dosis más alta (30 ug) en 16 a 25 años. La eficacia de ‘Comirnaty’ se calculó en casi 2.000 niños de 5 a 11 años que no presentaban signos de infección previa. Estos niños recibieron la vacuna o un placebo (una inyección ficticia).
De los 1.305 niños que recibieron la vacuna, tres desarrollaron COVID-19 en comparación con 16 de los 663 niños que recibieron placebo. Esto significa que, en este estudio, la vacuna tuvo una efectividad del 90,7% en la prevención del COVID-19 sintomático (aunque la tasa real podría estar entre el 67,7% y el 98,3%).
Los efectos secundarios más comunes en niños de 5 a 11 años son similares a los de las personas de 12 años o más. Incluyen dolor en el lugar de la inyección, cansancio, dolor de cabeza, enrojecimiento e hinchazón en el lugar de la inyección, dolor muscular y escalofríos. Estos efectos suelen ser leves o moderados y mejoran a los pocos días de la vacunación.
En cuanto a la seguridad y eficacia de la vacuna, tanto en niños como en adultos, desde el organismo de la EMA señalan que se seguirá supervisando de cerca, ya que se utiliza en campañas de vacunación en los Estados miembros de la UE a través del sistema de farmacovigilancia de la UE y los estudios en curso y adicionales realizados por la empresa y las autoridades europeas.